近日,中国农业科学院上海兽医研究所家禽病毒病监测预警和防控团队研究发现,RNA病毒感染可诱导关键的宿主因子DDX46发生蛋白切割,促使其从细胞核转移至细胞质。这一转位过程“解锁”了原本被扣押在核内的天然免疫信号分子,使其得以能够迅速翻译并启动早期抗病毒防御反应。相关研究成果发表于《mBio》。
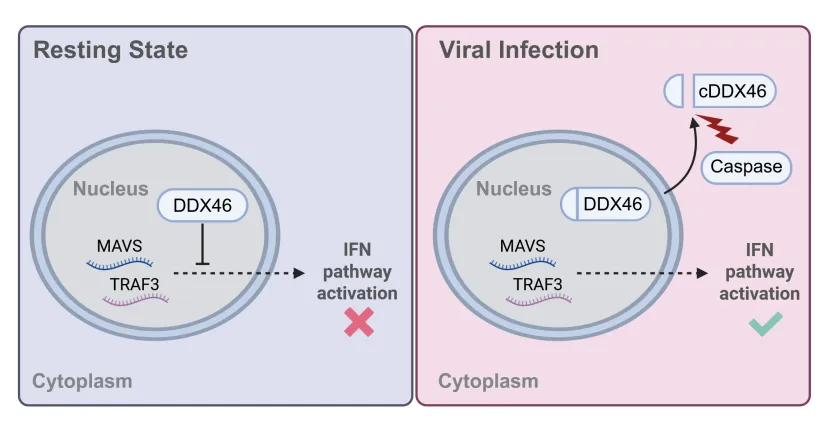
Caspase介导的DDX46切割“解锁”抗病毒免疫
DDX46属于DEAD/H-box RNA解旋酶家族成员。此前研究表明,DDX46可通过抑制先天免疫相关分子转录本出核,进而抑制干扰素产生,但其在病毒感染过程中的动态调控机制尚不明确。本研究通过针对RNA结合蛋白的CRISPR/Cas9筛选,首次鉴定出DDX46是RNA病毒复制所必需的关键宿主因子。进一步机制研究发现,RNA病毒感染可诱导DDX46在第226位天冬氨酸残基处发生Caspase依赖性切割。切割后的DDX46发生核质转位,解除其对天然免疫分子mRNA的核内滞留作用,从而显著增强干扰素等抗病毒分子的表达。
该研究阐明了RNA病毒感染通过Caspase依赖性翻译后修饰及亚细胞定位重塑,精确调控DDX46功能并放大抗病毒先天免疫反应的分子通路。相关发现不仅深化了对RNA解旋酶动态功能及宿主抗病毒免疫调控机制的认识,也为靶向宿主蛋白修饰过程开发新型抗病毒策略提供了理论依据基础。
中国农业科学院上海兽医研究所博士研究生刘彦峰为论文第一作者,孙英杰研究员为论文通讯作者。丁铲研究员为本研究提供了重要指导。该研究得到国家重点研发计划青年科学家项目、国家自然科学基金、中国农业科学院科学中心项目的资助。




